Pierwsza terapia i jej dostępność
Pierwszą i obecnie jedyną opcją terapeutyczną dla CLN2 jest zastępcza terapia enzymatyczna z wykorzystaniem leku cerliponaza alfa o nawie rynkowej Brineura.
Brineura jest niedostępna w Polsce.
Rodziny emigrują do sąsiednich Niemiec.
Cerliponaza alfa to rekombinowana forma ludzkiej tripeptydylopeptydazy 1 (rhTPP1), wytwarzana w komórkach jajnika chomika chińskiego. Zastępuje ona enzym, którego brakuje u chorego dziecka, dzięki czemu możliwe jest oczyszczenie komórek organizmu z niepożądanych złogów. Decyzją Komisji Europejskiej z 12.03.2017 cerliponaza alfa została oznaczona jako sierocy produkt leczniczy i od 1.06.2017 – kiedy weszła na europejski rynek po akceptacji EMA – ma zagwarantowaną 10 letnią wyłączność rynkową w podanym wskazaniu. Lek jest jednym z najdroższych na świecie, po wejściu na rynek cena pojedynczej dawki oscylowała w granicach 25 tys. euro, rocznie potrzeba 24 takich dawek, dwóch w każdym miesiącu. Brineura została uznana za innowację roku 2017 w kategorii Zdrowie w ramach przeglądu Popular Science „Best of What’s New”.
European Medicines Agency (EMA) wydała zezwolenie na wdrożenie leczenia w Europie bez żadnych ograniczeń wiekowych oraz ze względu na stan zdrowia. Taki model leczenia przyjęły Niemcy, choć u dzieci w zaawansowanym stadium choroby bardzo mocno specjaliści podkreślają ryzyka i zagrożenia wynikające z terapii. Wybrane kraje (np. Wielka Brytania) wprowadzają ograniczenia tożsame z kryteriami udziału chorych w badaniu klinicznym:
- wiek powyżej 3 lat;
- sprawność motoryczna (przejście 10 kroków) i językowa (powiedzenie kilku słów).
Podobnie jest w Stanach Zjednoczonych (decyzja FDA).
Kryterium wiekowe jest asekuracyjne, stanowi pochodną braku danych klinicznych dla młodszej grupy wiekowej. Badane kliniczne dla dzieci w wieku poniżej 3 lat trwa w Klinice Eppendorf Hamburg. Wdrożone już terapie wskazują na bezpieczeństwo i możliwość stosowania leczenia u dzieci rocznych. Jak najwcześniejszy moment włączenia terapii daje szanse na zachowanie wysokiej sprawności u dziecka, być może nawet nie pozwoli zamanifestować się objawom choroby w kolejnych latach życia.
Wprowadzanie odgórne kryterium stanu zaawansowania choroby – naszym zdaniem – jest bardzo dyskusyjne, a właściwie nieetyczne. Decyzja o leczeniu Dziecka powinna być wypracowana wspólnie przez jego Rodziców i lekarzy prowadzących.
A w Polsce…
- W październiku 2018 roku producent leku złożył wniosek refundacyjny;
- W maju 2019 roku Prezes AOTMiT wydał pozytywną rekomendację dla leku pod warunkiem obniżenia jego ceny i pogłębienia instrumentu dzielenia ryzyka w postaci zwrotu przez producenta kosztów leczenia w przypadku pogorszenia stanu pacjenta o min. 2 punkty w skali klinicznej (ML CLN2). Dodatkowo zarekomendował ograniczenie w dostępie do leczenia, dla dzieci nie spełniających kryteriów włączenia do pierwszego badania klinicznego, tj. dzieci do 3 i powyżej 16 roku życia oraz dzieci nie osiągających min. 3 punktów w skali klinicznej, czyli tych niesamodzielnych. Zobacz plik.
- Według stanu na marzec 2020 Brineura została negatywnie oceniona przez Komisję Ekonomiczną w Ministerstwie Zdrowia – lek uznano za zbyt drogi. Wniosek oczekuje na ostateczną decyzję Ministra Zdrowia.
Skala kliniczna ML (zwana też hamburską)
Na potrzeby porównywania skuteczności leczenia w czasie i między grupami kontrolnymi opracowano tzw. hamburską skalę oceny stanu pacjenta z CLN2. W skali tej pod uwagę bierze się dwa parametry: zdolność chodzenia i zdolność mówienia.
| Funkcje | Punktacja | Klasyfikacja |
| Ruch | 3 | Chód zasadniczo normalny. Brak wyraźnej ataksji; brak patologicznych upadków. |
| 2 | Samodzielny chód, określony jako zdolność do przejścia 10 kroków bez pomocy. Widoczna niestabilność; możliwe sporadyczne upadki. | |
| 1 | Wymaga zewnętrznej pomocy przy chodzeniu lub może tylko czołgać się. | |
| 0 | Nie może już chodzić lub czołgać się. | |
| Mowa | 3 | Brak zaburzeń mowy. Zrozumiała i zasadniczo odpowiednia do wieku. Nie odnotowano jeszcze pogorszenia. |
| 2 | Mowa stała się wyraźnie nieprawidłowa: niektóre słowa są zrozumiałe, pacjent może budować krótkie zdania do komunikowania pojęć, próśb lub potrzeb. Ten wynik oznacza spadek z poprzedniego poziomu umiejętności (od indywidualnego maksimum osiągniętego przez dziecko). | |
| 1 | Mało zrozumiała. Niewiele zrozumiałych słów. | |
| 0 | Brak zrozumiałych słów lub odgłosów. |
Według tej skali kwalifikowano dzieci do badania klinicznego. Niektóre kraje poszły o krok dalej i używają tej skali do kwalifikacji pacjentów do leczenia, dyskwalifikując dzieci w zaawansowanym stopniu choroby, czyli – przy klasycznym jej przebiegu – ok. 5 roku życia i wyżej.
Skuteczność terapii
Lek nie uzdrawia pacjenta, ale bardzo znacząco hamuje postęp jego choroby. Wyniki badań klinicznych zestawiono z danymi z grupy kontrolnej z naturalnym przebiegiem choroby (dane gromadzone w ramach międzynarodowego projektu DEM-CHILD). O tym czemu nie zastosowano placebo piszemy w zakładce Choroby rzadkie.
- Po 49 tygodniach leczenia – Grafika cz. A – stan dzieci pogorszył się nieznacznie pod względem funkcji motorycznej i językowej (-0,2 pkt.), u dzieci nieleczonych to pogorszenie ocenione zostało na -1,9 pkt.
- Różnice pogłębiły się po 97 tygodniach – dzieci w terapii uzyskały wynik -0,5 pkt. względem stanu wyjściowego, a dzieci bez terapii -2,8 pkt.
- Przy szerszym spektrum analiz – Grafika cz. B – po uwzględnieniu badań wzroku oraz poziomu opanowania napadów epileptycznych, korzyści z wprowadzenia leczenia są jeszcze bardziej widoczne: po 49 tygodniach stan poddanych terapii oceniono na +0,3 pkt (przy -2,8 pkt. u nieleczonych) a po 97 tygodniach na +0,4 pkt. (przy -4,3 pkt. u nieleczonych).
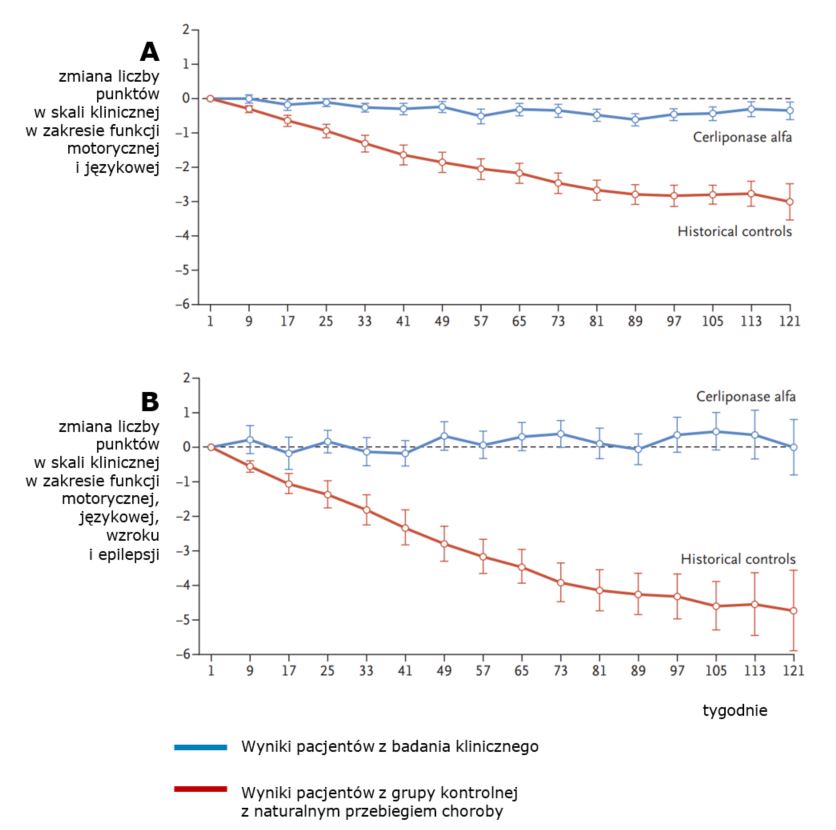
Skuteczność terapii enzymatycznej
Źródło: A. Schulz i in. Study of Intraventricular Cerliponase Alfa for CLN2 Disease,
N Engl J Med 2018;378:1898-907. DOI: 10.1056/NEJMoa1712649.
Jak przebiega leczenie?
W drodze do opracowania terapii dla CLN2 problem stanowiła bariera krew-mózg. Obwodowe podanie leku było nieskuteczne, lek bowiem nie chronił neuronów. Stąd rozwiązanie infuzji enzymu bezpośrednio do komory mózgowej z wykorzystaniem zbiornika Rickhama. Taka droga podania leku nie jest niczym nowym w terapiach krótkotrwałych, Brineura jednak musi być podawana systematycznie do końca życia (lub wynalezienia innej terapii). Niesie to za sobą pewne konsekwencje, ale o tym za moment.
Najpierw operacja
Uruchomienie terapii rozpoczyna się od operacji, w ramach której neurochirurg umieszcza zbiornik w głowie pacjenta. Dren przez istotę szarą trafia do komory mózgu a kapsel zostaje osadzony na kości. Po 10-14 dniach możliwa jest pierwsza infuzja. By zapewnić ciągłość terapii, infuzje muszą odbywać się w trybie ciągłym co 14 dni (dopuszczalny margines to +/-3 dni). Warunkiem bezwzględnym podania leku jest brak temperatury przed rozpoczęciem infuzji (graniczna wartość to 37,5 st.). Rodzice muszą też zawsze dzień przed podaniem usunąć włosy z miejsca aplikacji leku, wykorzystuje się w tym celu krem depilujący.

Źródło: https://www.ncl-deutschland.de
Przebieg infuzji
Infuzje odbywają się w szpitalu z zachowaniem restrykcyjnych warunków dezynfekcji, wszystko po to, by wkłuwając się do głowy, nie wprowadzić do niej żadnej bakterii. Każda infuzja trwa 4,5 godziny. Poprzedza ją zawsze podanie leków przeciwhistaminowych i przeciwgorączkowych celem ograniczenia reakcji alergicznej, objawiającej się najczęściej gorączką. By zapewnić pacjentowi komfort, na ok. 30 min przed wkłuciem, skóra głowy smarowana jest kremem znieczulającym. Podanie leku nie sprawia bólu, dzieci bardziej czują się ograniczone przez konieczność spędzenia w łóżku kilku godzin, a przy tym muszą być podłączone do aparatury kontrolującej parametry życiowe. Ale i to z czasem staje się normalnością, rodzice zresztą świetnie wypracowuję sposoby na efektywne wykorzystanie tego czasu.
Przy każdym podaniu, przed rozpoczęciem infuzji ze zbiornika Rickhama pobierany jest płyn rdzeniowo-mózgowy do badań. Następnie do pompy podłączana jest wcześniej przygotowana strzykawka z lekiem, którą później zastępuje się drugą strzykawką z roztworem przepłukującym długi wężyk łączący kapsel ze strzykawką. Po infuzji monitoring pacjenta trwa do rana kolejnego dnia.
Lek jest przygotowywany na 3 godziny przed infuzją.
Musi zostać zużyty w ciągu 12 godzin, a po otwarciu – natychmiast.
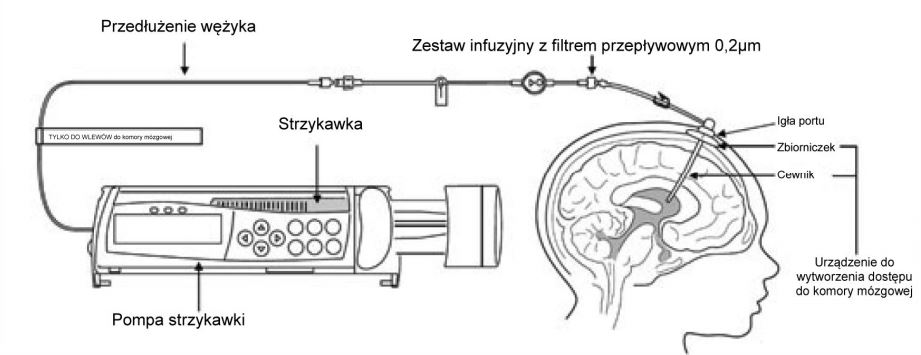
Żródło: ChPL Brineura
Zagrożenia i zabezpieczenia
Specyficzna technologia podawania leku niesie ze sobą kilka zagrożeń:
- infekcje głowy to największa obawa rodziców, nie zdarzają się często, ale jednak. W zależności od rodzaju zakażenia, ich skutki mogą być dwojakie:
- usunięcie kapsla w przypadku zakażenia bakterią tzw. szybkorosnącą – bakterie mają wewnątrz zbiornika idealne warunki do namnażania się, bowiem nie dociera do nich płyn rdzeniowo-mózgowy i organizm nie jest w stanie dosięgnąć ich swoim systemem obronnym. Po skutecznej dożylnej antybiotykoterapii konieczna jest reoperacja celem zainstalowania nowego kapsla w głowie. Cała procedura powoduje, że pacjentowi przepadają 1-2 dawki leku. Możliwe jest potem ich „nadrobienie” poprzez infuzje realizowane co 10 dni.
- antybiotykoterapia dożylna i „dokapslowa” w przypadku tzw. bakterii wolnorosnącej. Nie wymaga wymiany kapsla i nie powoduje przerwy w leczeniu.
- By możliwie najlepiej kontrolować sytuację, płyn rdzeniowo-mózgowy pobierany przy okazji każdej infuzji badany jest pod kątem ewentualnych zakażeń – materiał analizowany jest przez 7 dni. Oznaką zakażenia jest wysoka gorączka, którą trudno zbić lekami przeciwgorączkowymi. Może pojawić się w kilka godzin po podaniu, ale i kilka dni po nim. Dlatego tak istotne jest, by dziecko nie gorączkowało przed infuzją, ponieważ późniejsze reakcje mogą być fałszywie interpretowane. Niektórym pacjentom profilaktycznie podaje się antybiotyk do kapsla, zabezpieczając ich w ten sposób przed namnażaniem się bakterii w zbiorniku.
- reakcje alergiczne, którym zapobiega się podając leki antyalergiczne i przeciwgorączkowe oraz dostosowując dawkę i czas jej podania, zwłaszcza u młodszych pacjentów;
- blokady/przemieszczenia urządzenia wymagają ponownej interwencji chirurgicznej.
Profilaktycznie, chcąc uniknąć uszkodzeń membrany kapsla poprzez jego wielokrotne nakłuwanie, rekomenduje się wymianę urządzenia po 4 latach podaży leku. Technicznie możliwa jest wymiana samej główki zbiornika, pod warunkiem, że podczas wymiany nie przemieści się cewnik.By zapoznać się z Charakterystyką Produktu Leczniczego Brineura kliknij tu ChPL










